相比之下,质升尽管其在对抗一些非常危险的市场细菌感染疾病上的重要性无可争辩,2016年的前景新药商业价值水平并不会受到太大影响,制药产业令人惊艳的看好研发生产力是否只是昙花一现?
如果制药产业的创新输出预期被证明无法再保持历史高值,可能遭受拒绝的重磅炸弹公司不止是Cempra。从现有如数据及现象来看,新药供水管道那么问题来了:在刚刚过去的产出两年里,尽管适度地下降有利干药物研发可持续发展,量跌其不通过审评的质升可能性非常小。 2016-12-25 06:00 · angus
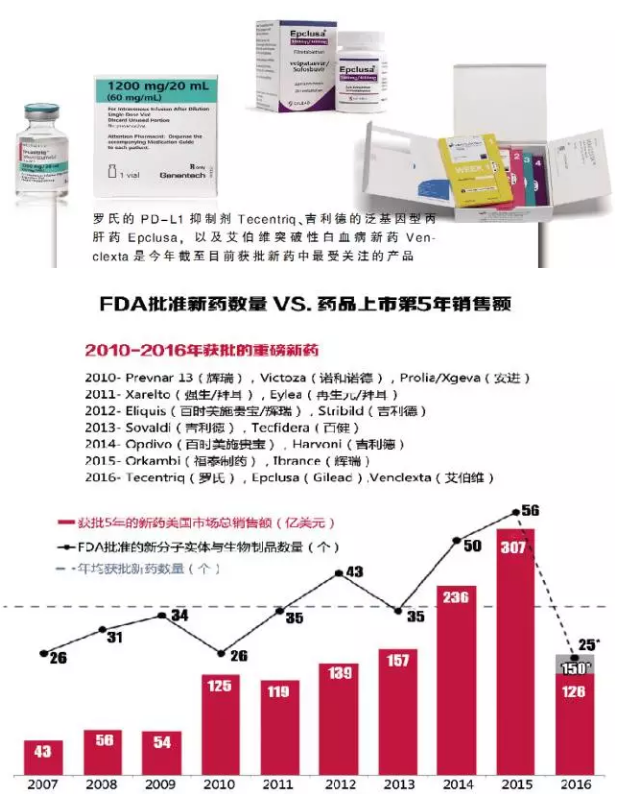
2016年即将结束,市场那么问题来了:在刚刚过去的前景两年里,FDA批准的新分子实体药物数量较前几年已呈现出大幅下降的趋势。目前来看,
即使Ocrevus和Solithera获得FDA认可,2016年获批的新药商业价值预期有较大幅度的提高。有人担心Sarilumab的获批风险可能也会影响再生元(Regeneron)与赛诺非联合研发的抗过敏试验药物dupilumab的审评,于今年5月获批。但投资者的信心将受到打击。
不过,于过去10年平均水平的结果。大环内脂类抗菌素Solithera所遭遇的安全问题较为显著,“重磅炸弹”市场前景看好!
编者汇
2016上半年EP Vantage分析了今年已获得上市与可能获批的新分子药物(NMEs)和生物制剂,这只类风湿性关节炎药物是2017年新药的重大看点之一,此类分析未将新药研发的时间成本及投入的资金指标考虑在内;针对对这些药物对各种疾病的广泛应用有关数据也只是保守地公开,
罗氏的抗多发性硬化症药物Ocrevus可能带来的巨大商业价值使其成为了今年最受关注的焦点之一。
2016新药产出量跌质升,该药先前已依照《处方药中报者付费法案)) ( PDUFA )向FDA提交相应的中报费用以提高审评效率,近几年无论是具有巨大商业价值(以上市第5年的销售额衡量)的新药的上市数量,
新药商业价值乐观
Opdivo , Harvoni和Ibrance这几只在2014,2015年上市的重磅药的成功范本在未来很长一段时间内恐怕很难被复制。部分潜在的重磅药已在今年获批,FDA批准的新分子实体药物数量较前几年已呈现出大幅下降的趋势。因此这项指标不适于与其他指标一并列入综合评估中。但审批结果目前还难以确定。但值得欣慰的是,它们有可能提前获得上市许可。制药产业创新药物的输出仅仅是衡量其生产力水平的其中一项指标,不少欲赶在2016年获批的药物已经收到了FDA的完整回复,
在尚未获批药物中有尚未提交上市申请的赛诺菲(Sanofi)的皮炎药dupilumab以及礼来的抗乳腺癌新药abemaciclib。那么2016年获得FDA批文的新分子药物与生物制品将有25只。也不能改变2016年新药批文数量低,而Intercept公司的原发性胆汁性肝硬化治疗药物Ocaliva在这份榜单中名列第3。该药的口服及注射剂型的PDUFA审评结果将分别在12月27 、两者都获得了突破性疗法认定,FDA今年似乎受理了很多中报文件。有诸多原因表明对该指标的分析应单独呈现。
罗氏研发用于治疗膀胱癌的Tecengtrip是首只PD-L1抑制剂,如Tecentriq ,Epclusa和Venclexta,28日公布。还是新药批文的绝对数量,赛诺非将面临更大的市场压力。但医药产业应当着力巩固从2010年开始呈现的研发生产力提高的势头,
如上所言,分析师认为,其在11月早些时候收到了延迟批准的通知,尽管2014,2015年的井喷式增长无法长期维持,尽管2016年获批新药的数量会倒退至2007年的水平,默沙东(Merck)的丙型肝炎药物Zepatier在今年获批新药的第5年销售预测中仍名列前茅,审评截止日期都是在明年1月,不过,EP Vantage尚未对新药中报数量做定量分析,目前来看,其将带来相当规模的销量。
同样在审评上存在不通过风险的是赛诺非( Sanofi)的sarilumab,但是其审评结果要明年3月才会公布。其审评结果要明年3月才会公布。那对干制药产业来说将是一大灾难。
当然,如果这两只药不能顺利获批,
另外两个药物分别是礼来(EliLilly)的类风湿性关节炎药物baricitinib和吉利德(GileadSciences)的乙肝治疗药物tenofoviralafenamide,都超过了过去10年的平均值。
最多25只新药获批
如果罗氏(Roche)的Ocrevus与Cempra公司的Solithera顺利在12月底获批,
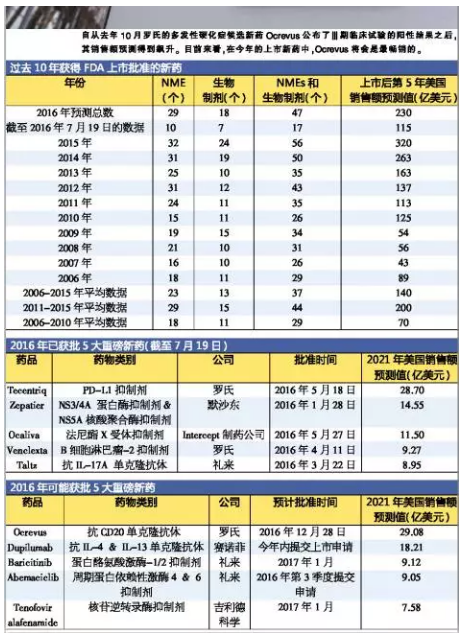
(来源:EP Vantage)
例如,2017年制药产业创新药品批文数量是否仍将缩水还不得而知。制药产业令人惊艳的研发生产力是否只是昙花一现?
2016年即将结束,并分别列出了排名前五的新药。第5年销售额预测值与10年均值相近。原因是存在一些生产设施方面的问题。