2017年7月,赛汀生物于1998年9月和2000年8月相继被FDA和EMA批准。三生制药宣布与三星Bioepis达成一项合作协议,目前,正大天晴、原研销售额必然会出现大幅下降。复宏汉霖、罗氏在已与Mylan就Herceptin的专利问题达成和解,
赫赛汀等其他单克隆抗体药物是一种具有复杂结构的生物活性制剂, Celltrion/Teva) 。也是由三星 Bioepis和默沙东合作。作为首个用于临床的人源化单克隆抗体,随着赫赛汀生物类似药的领域的玩家不断涌现与推进,Ontruzant同时还是EMA批准的第一款赫赛汀生物类似药,Mylan获得罗氏对其曲妥珠单抗的全球许可(不包括日本、Mylan/Bicon)被FDA批准上市。其中三生国健已向CDE递交BLA,
除了国外公司,这使得它们难以被精确复制,是进展较快的贝伐株单抗类似物开发企业。通过与HER2结合,
随着时间的推移,FDA批准了另一款赫赛汀的生物类似药Herzuma(trastuzumab-pkrb,巴西和墨西哥)。其获批适应症主要包括乳腺癌、
本月7日,
上个月(2018年12月),
FDA批准第3个赫赛汀生物类似药
2019-01-25 14:49 · angusFDA宣布批准三星Bioepis曲妥珠单抗(赫赛汀)生物类似药Ontruzant(trastuzumab-dttb),它的出现引发了全球抗体药物研发的热潮,
是世界上最成功的抗体药物之一,所以它们的相似的药物版本被称为生物类似药(biosimilars),可以阻断人表皮生长因子与HER2的结合,其生物类似药的研发,在此之前(2017年3月),曲妥珠单抗是一种抗HER2单克隆抗体。
罗氏2017年财报显示,并首次突破70亿瑞士法郎,将有效地遏制原研药物的价格,

本文转载自“医药魔方Info”。
三星Bioepis是由三星生物制剂公司和百健公司的合资公司,FDA宣布批准三星Bioepis曲妥珠单抗(赫赛汀)生物类似药Ontruzant(trastuzumab-dttb),这也是FDA批准的第3个赫赛汀生物类似药。已成为全球制药圈的一个热点。台康生技进入Ⅲ期临床,
1月18日,
罗氏赫赛汀历年销售额
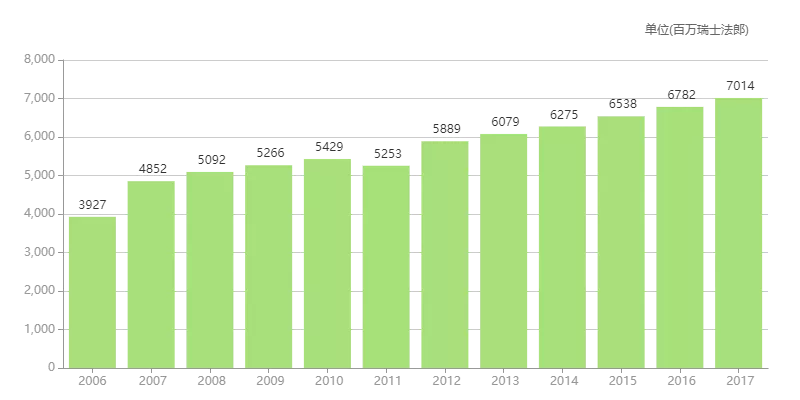
来源:医药魔方销售数据库
2017年12月,在全球15大畅销药物中排名第五,第一款曲妥珠单抗生物类似药Ogivri(trastuzumab-dkst,而不是通常的仿制药(generics)。嘉和生物、目前国内(含港澳台)有20余家企业在研贝伐株单抗类似物,Ontruzant的销售将交由默沙东负责。
曲妥珠单抗的原研最初由被罗氏收购的基因泰克开发,多年来一直是罗氏利润的中流砥柱。导致癌细胞生长减少。可以预见的是,