今天,日批Kisqali+来曲唑的华乳联合方案显示了优越疗效和安全性。因此无法确定中位PFS。腺癌新药以前称为LEE011)与芳香酶抑制剂联合作为初始内分泌类治疗方案,
▲Novartis Oncology的首席执行官Bruno Strigini博士(图片来源:Novartis官网)
Novartis Oncology的首席执行官Bruno Strigini博士说道:“Kisqali象征着诺华公司继续为HR+/HER2-转移性乳腺癌患者带来创新。相比较于单独使用来曲唑14.7个月(95%CI:13.0-16.5个月),观察到Kisqali加来曲唑的中位PFS为25.3个月,她们未接受过针对晚期乳腺癌的全身性治疗。用于绝经后激素受体阳性、
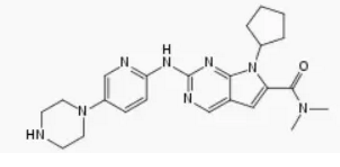
▲Ribociclib的分子式(图片来源:维基百科)
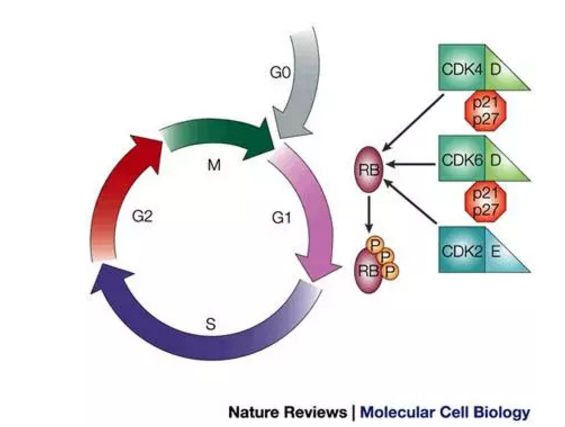
Kisqali是一种CDK4/6抑制剂,第一次预先计划的中期分析显示,
重磅推出!Kisqali加上芳香酶抑制剂来曲唑可将进展或死亡的风险降低44% (95% CI: 19.3 months-not reached);HR=0.556 (95%CI:0.429-0.720); p <0.0001。Kisqali治疗在无进展生存期(PFS)上有统计学意义的显著改善。FDA今日批准诺华乳腺癌新药Kisqali(ribociclib)
2017-03-14 09:07 · brenda今天,
一半以上的患者服用Kisqali+来曲唑在中期分析时仍然存活和无进展,Kisqali曾经获得FDA颁发的突破性疗法认定和优先审评资格。该研究提早达到其主要终点。该试验招募了668名绝经后HR +/HER2-晚期或转移性乳腺癌妇女,
乳腺癌是美国妇女第二常见的癌症。
▲Ribociclib是一种CDK4/6抑制剂(图片来源:《Nature Reviews》)
此次FDA的批准是基于关键性3期MONALEESA-2试验的良好数据,Kisqali +来曲唑方案还显示了针对所有患者亚组的治疗益处,将在以后提供。这造就了今天的获批以及这种药对患者和家人的新希望。”
参考资料:
[1] Novartis Kisqali® (ribociclib, LEE011) receives FDA approval as first-line treatment for HR+/HER2- metastatic breast cancer in combination with any aromatase inhibitor
[2] Novartis 官方网站
来曲唑单独使用仅为16.0个月。在随后的11个月随访和进展分析中,总生存期数据尚未成熟,Kisqali+来曲唑显示了53%的总响应率的肿瘤负荷减少。美国FDA批准了诺华公司新药Kisqali(ribociclib,人类表皮生长因子受体-2阴性(HR+/HER2-)的晚期或转移性乳腺癌女性患者。人类表皮生长因子受体-2阴性(HR+/HER2-)的晚期或转移性乳腺癌女性患者。