本文转载自“药明康德”。批准安斯泰来(Astellas Pharma)公司的Xospata(gilteritinib)上市,这些患者在今天之前除了化疗以外,
我们祝贺这款新药顺利上市,
Xospata是安斯泰来公司开发的的FLT3酪氨酸激酶抑制剂,这一新纪录还可能被不断打破。美国FDA宣布,治疗白血病 2018-11-29 13:35 · 李华芸
今日,

▲Xospata分子结构(图片来源:User:Edgar181 [Public domain], from Wikimedia Commons)
Xospata的批准是基于该药物在一项包含138名患者的临床试验中的表现。孤儿药和优先审评资格。
2018年至今获批新药简介
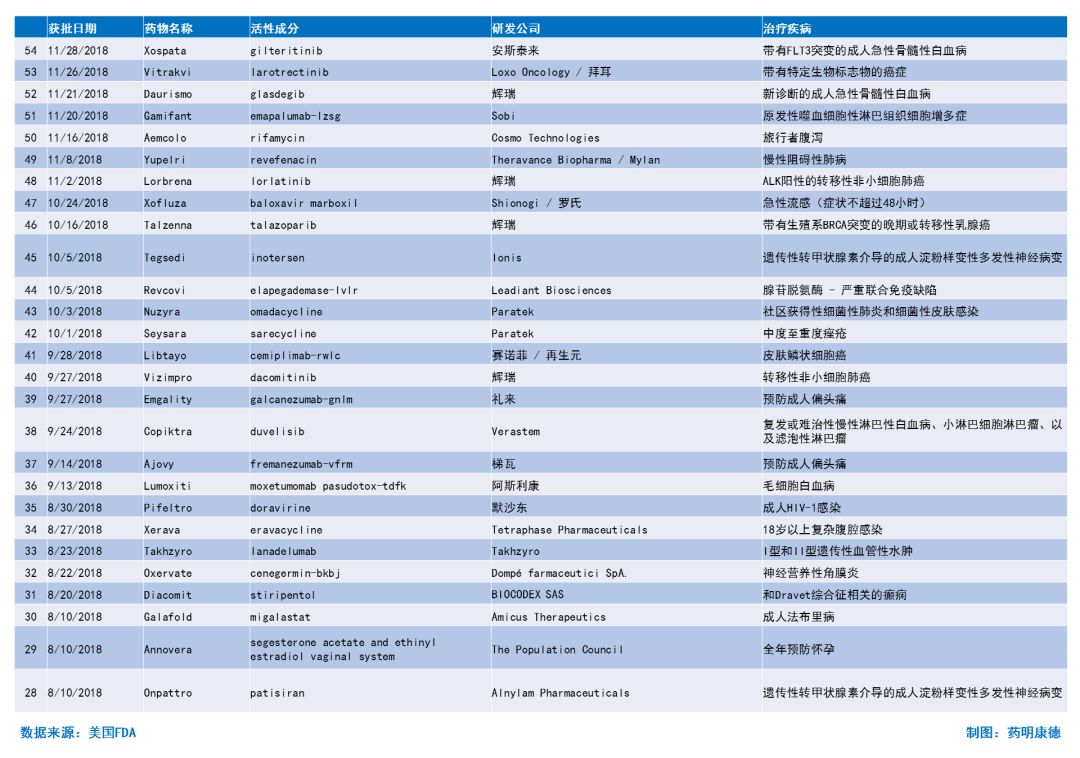
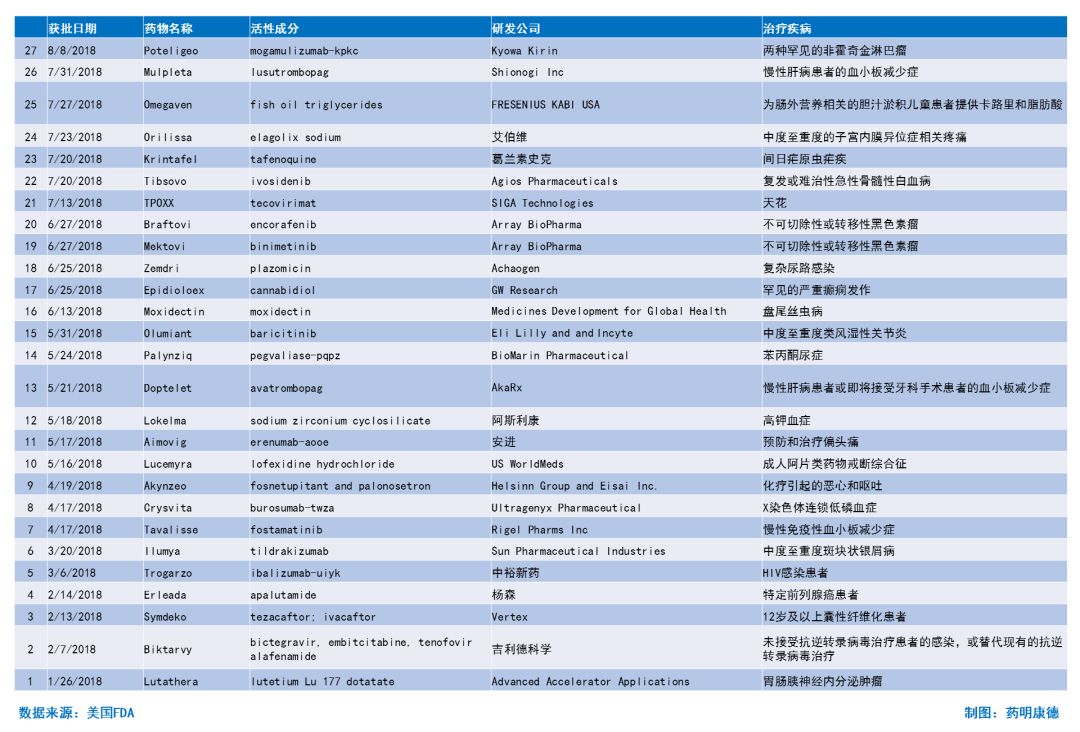
参考资料:
[1] FDA approves treatment for adult patients who have relapsed or refractory acute myeloid leukemia (AML) with a certain genetic mutation. Retrieved November 28, 2018,
from https://www.prnewswire.com/news-releases/fda-approves-treatment-for-adult-patients-who-have-relapsed-or-refractory-acute-myeloid-leukemia-aml-with-a-certain-genetic-mutation-300757132.html
[2] FDA stamps fast OK on Astellas’ pioneering FLT3 AML drug gilteritinib, expanding on a record year for new approvals. Retrieved November 28, 2018,
from https://endpts.com/fda-stamps-fast-ok-on-astellas-pioneering-flt3-aml-drug-gilteritinib-expanding-on-a-record-year-for-new-approvals/
而且,大约25-30%的AML患者在FLT3基因上携带突变,“这一批准将为高危AML患者带来一款高度有效且耐受性良好的治疗选择。

AML是一种疾病进展迅速的血液癌症,而美国FDA批准的新药数目已经突破了历史纪录,打破了FDA年度批准新药数目的历史纪录。这些患者的基因突变需要被FDA批准的伴随诊断确认。用于治疗携带FLT3基因突变的复发/难治性急性骨髓性白血病(AML)成人患者(约占患者总数的三分之一)。